| Guide | Identifier les parasites internes (à l’aide d’un microscope) |
| Groupe cible | Corvidés |
| Auteurs | helpthecrows@gmail.com |
| Version | 2022-04-26 |
| NOTE: In all my guides, I start from a situation where a rehabilitator takes his responsibility to take care of the animals in an ethically correct way. You should always try to minimize stress for the bird and since the birds, just like humans, are not the same, it can mean that you handle a problem in different ways by being creative! If I see different ways of doing the same thing, I try to write it down in my guides, but it is always up to the rehabilitator to take their own responsibility. I do not have to write « I recommend putting the bird down » or « contact a veterinarian » or « according to law, you should … » because I start from the situation where you do the best for the bird and that you as a rehabilitator have learned to draw the line so that you do not end up in an unwanted or illegal situation. There may be an eternal battle between what you want and what is best for the bird. There are also many factors where a similar situation can give different results. For example: access to a veterinarian, lack of time, lack of knowledge and previous experience can include cause large differences in the treatment and decision-making process and indirectly also the end result. Knowledge of basic things can make a huge difference in the stress level of the crow. For example. avoid anything that is black or checkered. They do not like it instinctively and it creates stress when they see that you are dealing with something that is black. I put energy into my guides to make it easier for a rehabilitator to find information and to spread knowledge. Do you see a way to improve my guides or do you see a mistake or do you want to add something, feel free to inform me! If you are worried about doing something because it is new, ask other rehabilitators or a veterinarian for help. The guides are continuously updated, so make sure to always download the latest version from www.corvidlove.com |
Ce guide décrit comment détecter les parasites courants des corneilles à l’aide d’un microscope.
Il existe deux manières différentes de prélever un échantillon qui est ensuite analysé au microscope.
Méthode 1)Utiliser une goutte de solution saline
– Prenez des selles de l’oiseau (environ la moitié d’une tête d’allumette)
– Mettez-le sur une diapositive propre
– Prendre une goutte de sérum physiologique stérile (solution saline, la plus simple à trouver en pharmacie) et déposer la goutte sur l’échantillon de selles
– Remuez un peu à l’aide d’un bâton en bois ou du dos d’une allumette. Le mieux est bien sûr d’acheter des cure-dents emballés individuellement, mais ils ne sont peut-être pas si faciles à se procurer.
– Placez une lamelle dessus et assurez-vous qu’elle est complètement à plat sur la lame
– Vous êtes maintenant prêt à analyser l’échantillon au microscope.
Méthode 2)Utilisation de la « méthode de flottation »
Un gros avantage de cette méthode est qu’il est plus facile de trouver des parasites car vous obtenez une concentration plus élevée de parasites/œufs de parasites.
Il faut d’abord préparer un liquide de flottation avec du sel ou du sel et du sucre ou en utilisant du nitrate (c’est mieux)
- Solution saline saturée
4 grammes de sel dans 10 ml d’eau chaude ou chaude
Bien mélanger avant utilisation.
- Solution sel/sucre
Chlorure de sodium: 4 grammes
Eau: 10 ml d’eau chaude ou bouillante
Sucre: 5 grammes
Dissoudre le sel dans l’eau pour obtenir une solution saturée.
Remuez bien.
Ajoutez le sucre à la saumure saturée.
Remuer jusqu’à ce que le sucre soit dissous.
REMARQUE: Des cristaux peuvent se former si vous attendez plus de 20 minutes.
3.Solution de nitrate
Nitrate (NaNO3): 4 grammes
Eau: 10 ml
Prendre d’abord de l’eau, et en remuant, pour compléter avec les nitrates
Si vous trouvez un produit assurez-vous qu’il s’agit bien du Nitrate de Sodium (Nitrate de Sodium) car le Nitrate peut aussi être autre chose!
Prenez un petit verre/éprouvette (de préférence pas plus large qu’une lame) et remplissez-le à moitié avec la solution que vous avez préparée + ajoutez des fientes d’oiseaux (prenez d’abord un petit morceau et mélangez, ajoutez-en un peu plus et mélangez, etc. jusqu’à ce que le liquide ait clairement pris une couleur différente.
Ajoutez maintenant la solution sur le bord afin qu’elle dépasse un peu en haut mais pas au point de déborder. Si vous rencontrez des difficultés pour obtenir ce résultat, vous pouvez utiliser une seringue ou une pipette.
Placez maintenant une diapositive dessus (voir photo) et attendez environ 10 minutes.
Soulevez la lame et recouvrez-la d’une lamelle.

Vous pouvez enfin continuer à analyser les résultats au microscope.
Ascaris / ver enroulé(œufs de…)
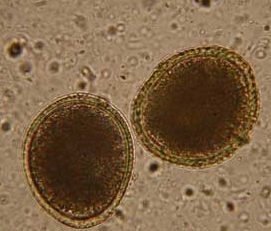
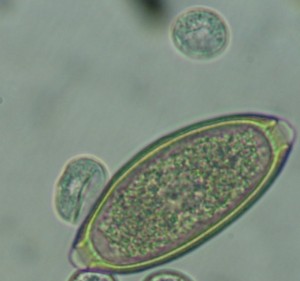
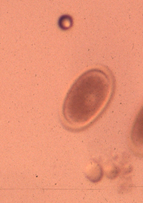
Les vers ronds sont généralement ovales et possèdent une double paroi cellulaire. Le plus souvent, ils créent des problèmes au niveau du tractus gastro-intestinal. Certaines espèces communes sont: « Ascardia spp », « heterakis gallinarum », « Strongyloides spp » et « capillaria spp ».
Ver d’espace(Oeuf de Syngamus trachée)

Le ver est situé dans la trachée de l’oiseau (trachée) et rend la respiration de l’oiseau difficile.
Ténias(Oeufs de Cesoda)
Google « ténia aviaire » si vous voulez voir plus de photos
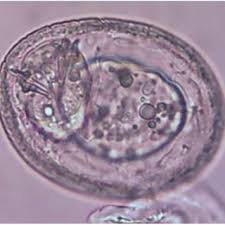
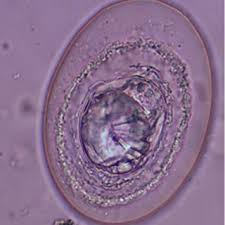
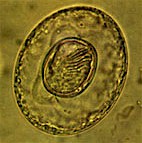
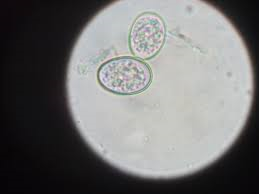
Coccidies(l’infection s’appelle coccidiose)
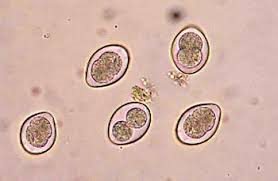
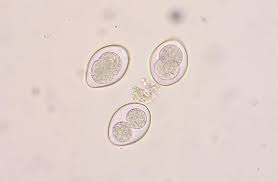
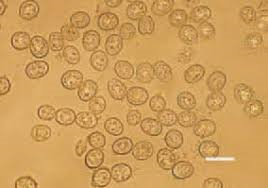
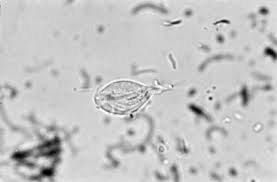
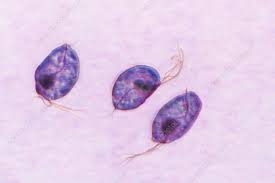
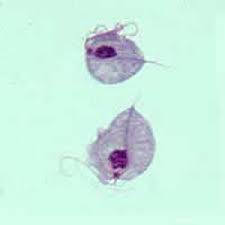
Trichomonas gallinae(Trichomonose)
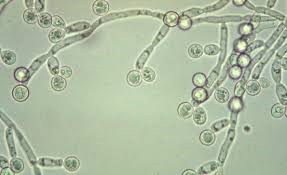
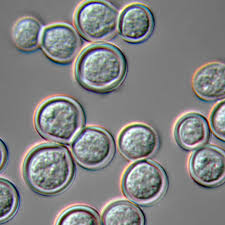
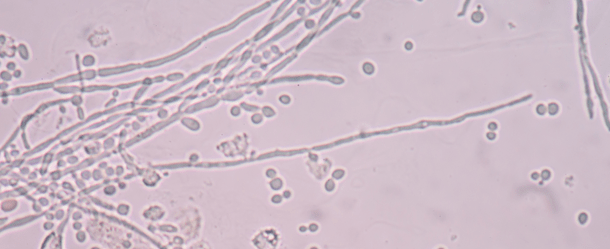
Champignon de levure(divers parasites: candida, aspergillus, cryptococcus et malassezia)