| Guide | Identifier les parasites internes (à l’aide d’un microscope) |
| Groupe cible | Corvidés |
| Auteurs | helpthecrows@gmail.com |
| Version | 2022-04-26 |
| REMARQUE : Dans tous mes guides, je pars du principe qu’un soigneur ou réhabilitateur prend la responsabilité de s’occuper des animaux d’une manière éthique. Il faut toujours essayer de réduire le stress de l’oiseau autant que possible. Comme les oiseaux, tout comme les humains, ne sont pas tous identiques, il peut être nécessaire d’aborder un problème de différentes façons en faisant preuve de créativité. Si je vois plusieurs façons de faire la même chose, j’essaie de les noter dans mes guides, mais il appartient toujours au réhabilitateur de prendre ses propres responsabilités. Je n’ai pas besoin d’écrire à chaque fois « je recommande d’euthanasier l’oiseau », « contactez un vétérinaire » ou « selon la loi, vous devez… », car je pars de la situation où vous faites ce qui est le mieux pour l’oiseau et où, en tant que réhabilitateur, vous avez appris à fixer les limites nécessaires pour ne pas vous retrouver dans une situation indésirable ou illégale. Il peut exister un conflit permanent entre ce que l’on veut faire et ce qui est le mieux pour l’oiseau. De nombreux facteurs peuvent aussi faire qu’une situation semblable donne des résultats différents. Par exemple : l’accès à un vétérinaire, le manque de temps, le manque de connaissances et l’expérience antérieure peuvent entraîner de grandes différences dans le traitement, le processus de décision et, indirectement, le résultat final. Connaître les bases peut faire une énorme différence dans le niveau de stress de la corneille. Par exemple, évitez tout ce qui est noir ou à carreaux. Les oiseaux n’aiment pas cela instinctivement, et cela crée du stress lorsqu’ils vous voient manipuler quelque chose de noir. Je consacre beaucoup d’énergie à mes guides afin qu’il soit plus facile pour un réhabilitateur de trouver des informations et de diffuser les connaissances. Si vous voyez une façon d’améliorer mes guides, si vous remarquez une erreur ou si vous souhaitez ajouter quelque chose, n’hésitez pas à m’en informer. Si vous hésitez à faire quelque chose parce que c’est nouveau pour vous, demandez de l’aide à d’autres réhabilitateurs ou à un vétérinaire. Les guides sont continuellement mis à jour ; veillez donc à toujours télécharger la dernière version depuis www.corvidlove.com. |
Ce guide décrit comment détecter les parasites courants des corneilles à l’aide d’un microscope.
Il existe deux manières différentes de prélever un échantillon qui est ensuite analysé au microscope.
Méthode 1)Utiliser une goutte de solution saline
– Prenez des selles de l’oiseau (environ la moitié d’une tête d’allumette)
– Mettez-le sur une diapositive propre
– Prendre une goutte de sérum physiologique stérile (solution saline, la plus simple à trouver en pharmacie) et déposer la goutte sur l’échantillon de selles
– Remuez un peu à l’aide d’un bâton en bois ou du dos d’une allumette. Le mieux est bien sûr d’acheter des cure-dents emballés individuellement, mais ils ne sont peut-être pas si faciles à se procurer.
– Placez une lamelle dessus et assurez-vous qu’elle est complètement à plat sur la lame
– Vous êtes maintenant prêt à analyser l’échantillon au microscope.
Méthode 2)Utilisation de la « méthode de flottation »
Un gros avantage de cette méthode est qu’il est plus facile de trouver des parasites car vous obtenez une concentration plus élevée de parasites/œufs de parasites.
Il faut d’abord préparer un liquide de flottation avec du sel ou du sel et du sucre ou en utilisant du nitrate (c’est mieux)
- Solution saline saturée
4 grammes de sel dans 10 ml d’eau chaude ou chaude
Bien mélanger avant utilisation.
- Solution sel/sucre
Chlorure de sodium: 4 grammes
Eau: 10 ml d’eau chaude ou bouillante
Sucre: 5 grammes
Dissoudre le sel dans l’eau pour obtenir une solution saturée.
Remuez bien.
Ajoutez le sucre à la saumure saturée.
Remuer jusqu’à ce que le sucre soit dissous.
REMARQUE: Des cristaux peuvent se former si vous attendez plus de 20 minutes.
3.Solution de nitrate
Nitrate (NaNO3): 4 grammes
Eau: 10 ml
Prendre d’abord de l’eau, et en remuant, pour compléter avec les nitrates
Si vous trouvez un produit assurez-vous qu’il s’agit bien du Nitrate de Sodium (Nitrate de Sodium) car le Nitrate peut aussi être autre chose!
Prenez un petit verre/éprouvette (de préférence pas plus large qu’une lame) et remplissez-le à moitié avec la solution que vous avez préparée + ajoutez des fientes d’oiseaux (prenez d’abord un petit morceau et mélangez, ajoutez-en un peu plus et mélangez, etc. jusqu’à ce que le liquide ait clairement pris une couleur différente.
Ajoutez maintenant la solution sur le bord afin qu’elle dépasse un peu en haut mais pas au point de déborder. Si vous rencontrez des difficultés pour obtenir ce résultat, vous pouvez utiliser une seringue ou une pipette.
Placez maintenant une diapositive dessus (voir photo) et attendez environ 10 minutes.
Soulevez la lame et recouvrez-la d’une lamelle.

Vous pouvez enfin continuer à analyser les résultats au microscope.
Ascaris / ver enroulé(œufs de…)
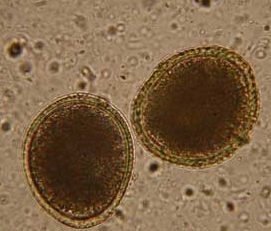
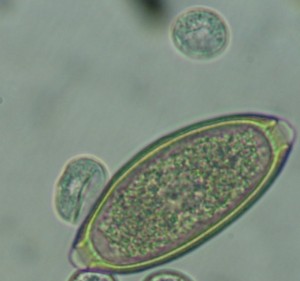
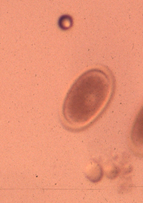
Les vers ronds sont généralement ovales et possèdent une double paroi cellulaire. Le plus souvent, ils créent des problèmes au niveau du tractus gastro-intestinal. Certaines espèces communes sont: « Ascardia spp », « heterakis gallinarum », « Strongyloides spp » et « capillaria spp ».
Ver d’espace(Oeuf de Syngamus trachée)

Le ver est situé dans la trachée de l’oiseau (trachée) et rend la respiration de l’oiseau difficile.
Ténias(Oeufs de Cesoda)
Google « ténia aviaire » si vous voulez voir plus de photos
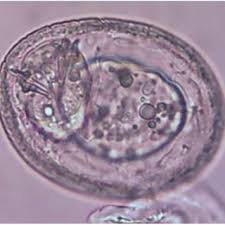
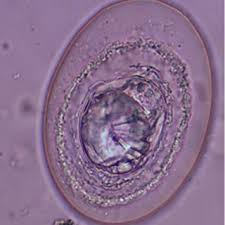
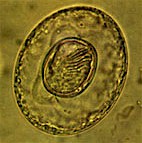
Coccidies(l’infection s’appelle coccidiose)
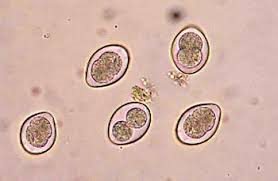
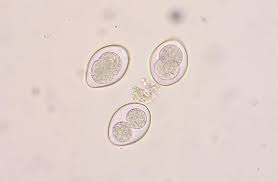
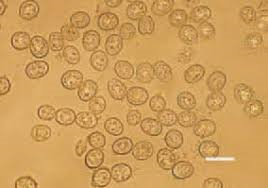
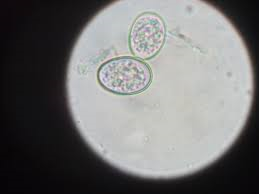
Trichomonas gallinae(Trichomonose)
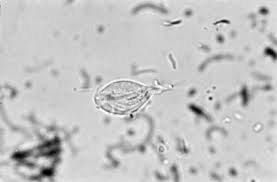
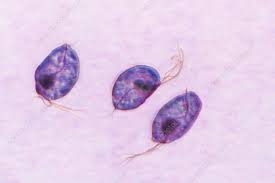
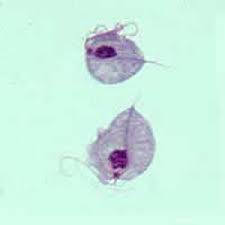
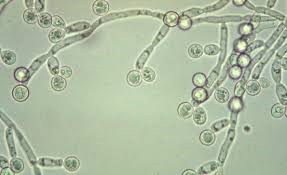
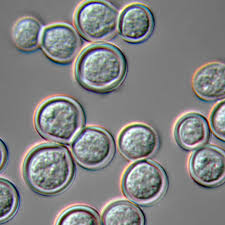
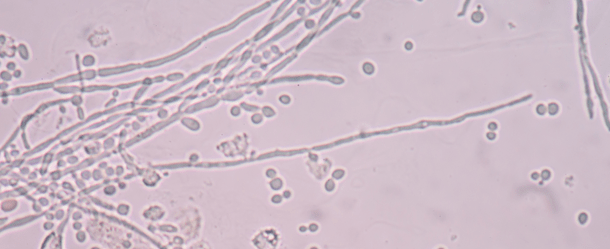
Champignon de levure(divers parasites: candida, aspergillus, cryptococcus et malassezia)